Луїджі Ріккарді 1 , Роза Маццео 2,*© , Анджело Раffеле Маркотриджано 1 , Гульєльмо Райнальді 3 , Паоло Іов'єно 4 , Віто Зонно 1 , Стефано Паван 1© і Кончетта Лотті 2,*
- 1 Відділ наук про ґрунт, рослини та харчові продукти, Відділ генетики рослин і селекції Університету Барі, Via Amendola 165/A, 70125 Bari, Італія; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (ARM); vito.zonno@uniba.it (ВЗ); stefano.pavan@uniba.it (SP)
- 2 Департамент наук про сільське господарство, продовольство та навколишнє середовище, Університет Фоджії, Віа Наполі 25, 71122 Фоджа, Італія
- 3 Департамент біологічних наук, біотехнологій та біофармацевтики, Університет Барі, Via Orabona 4, 70125 Bari, Італія; guglielmo.rainaldi@uniba.it
- 4 Департамент енергетичних технологій, відділ біоенергетики, біопереробки та зеленої хімії, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Італія; paolo.iovieno@enea.it
* Листування: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Анотація:
Лук (Allium cepa L.) є другою за значенням овочевою культурою в усьому світі і широко цінується за її користь для здоров’я. Незважаючи на значне економічне значення та цінність як функціонального продукту харчування, генетичне різноманіття цибулі мало вивчено. Тут ми досліджували генетичні варіації «червоної цибулі Acquaviva» (ARO), місцевого сорту зі столітньою історією вирощування в невеликому містечку в провінції Барі (Апулія, південь Італії). Набір з 11 мікросателітних маркерів використовувався для дослідження генетичної варіації в колекції зародкової плазми, що складається з 13 популяцій ARO і трьох поширених комерційних типів. Аналіз генетичної структури за допомогою параметричних і непараметричних методів підкреслив, що ARO являє собою чітко визначений генофонд, який чітко відрізняється від старовинних сортів Tropea і Montoro, з якими його часто помилково приймають. Для того, щоб дати опис цибулин, які зазвичай використовуються для споживання у свіжому вигляді, було оцінено вміст розчинної твердої речовини та гостроту, що показало вищу солодкість ARO порівняно з двома вищезгаданими старовинними сортами. Загалом, дане дослідження є корисним для майбутньої валоризації ARO, яку можна просувати через маркування якості, що може сприяти обмеженню комерційного шахрайства та покращенню доходів дрібних власників.
Вступ
Рід Лук налічує близько 750 видів [1], серед яких одним із найпоширеніших є цибуля (Allium cepa L., 2n = 2x =16). A. cepa має дворічний цикл і ауткросинг репродуктивну поведінку. Нині світове виробництво цибулі (97.9 млн. т) робить її другою за значенням овочевою культурою після томатів [2]. З давніх часів цибулю ріпчастої цибулі використовували як в їжу, так і в народній медицині. Дійсно, стародавні єгиптяни вже повідомляли про декілька терапевтичних формул, заснованих на використанні часнику та цибулі, у медичному папірусі 1550 року до нашої ери, Кодексі Еберса [3].
Цей універсальний і корисний овоч споживають у сирому, свіжому або переробленому вигляді, а також використовують для покращення смаку багатьох страв. Кілька останніх досліджень стверджують, що споживання цибулі може знизити ризик серцево-судинних захворювань [4,5], ожиріння [6], діабету [7] і різних форм раку [8–10]. Цілющі властивості цибулі часто пояснюють високим рівнем двох класів нутрицевтичних сполук: флавоноїдів і алк(ен)ілцистеїнсульфоксидів (ACSO). До першого класу відносяться флавоноли і антоціани. Кверцетин є основним виявленим флавонолом, відомим своїми сильними антиоксидантними та протизапальними властивостями у поглинанні вільних радикалів і зв’язуванні іонів перехідних металів. [11]; тоді як антоціани надають червоно-фіолетового кольору деяким сортам цибулі. Що стосується ACSO, найбільш поширеним є ізоалліїн [(+)-транс-S-1-пропеніл-L-цистеїну сульфоксид] [12], нелетка і непротеїногенна сірчана амінокислота, що зберігається в клітинах, яка опосередковано відповідає за гострий аромат і смак цибулі [13]. Під час руйнування тканини ізоаліїн розщеплюється ферментом аліїназою з утворенням ряду летких сполук (пірувату, аміаку, тіосульфонатів і пропанетіального S-оксиду), які викликають сльозотечу та викликають неприємний запах (гостроту). [14]. Гостроту цибулі часто вимірюють як кількість на грам свіжої ваги піровиноградної кислоти, що утворюється в результаті гідролізу. [15,16].
У країнах Середземноморського басейну запропонований як один із вторинних центрів різноманітності A. cepa [17,18], цибулини цибулі відрізняються великою різноманітністю форми, розміру, кольору, сухої речовини та гостроти [19-22]. Крім того, добриво на основі сірки, агротехнічні прийоми, тип ґрунту, кліматичні умови та генотип сортів або місцевих сортів можуть впливати на якість цибулини, надаючи особливі органолептичні та поживні властивості. [23-27]. В Італії, незважаючи на широку доступність зародкової плазми цибулі, лише кілька сортів цибулі часто піддаються науковим дослідженням і належним чином характеризуються [28,29].
Ретельна генетична та фенотипова характеристика агробіорізноманіття має вирішальне значення для забезпечення відповідного збереження генетичних ресурсів рослин і сприяння використанню конкретних генотипів у ланцюжку створення вартості [30-32]. Для картографування часто вибирають маркери простого повторення послідовності (SSR). [33-35], відбитки ДНК і розрізнення сортів [36-38], а також надійну оцінку генетичної мінливості всередині та між старовинними сортами [39-42], оскільки вони є локус-специфічними, мультиалельними, кодімінантно успадкованими, високовідтворюваними та придатними для автоматизованого генотипування.
У цьому дослідженні ми зосередили нашу увагу на традиційному місцевому сорті Апулії, «червоній цибулі Аквавіва» (ARO), який культивується відповідно до методів органічного землеробства в невеликій території міста Аквавіва делле Фонті, в провінції Барі. (Апулія, Південна Італія). Цибулини цього ландрасу великі, сплюснуті та червоного кольору, і в основному використовуються в місцевих рецептах. Незважаючи на те, що ARO отримав знак якості «Slow Food Presidium», його продукція може бути додатково просувана та захищена знаками якості Європейського Союзу, такими як захищене географічне зазначення (PGI) та захищене позначення походження (POD), оскільки це може сприяти обмеженню комерційне шахрайство та підвищення доходів дрібних власників. Тут молекулярні маркери SSR були використані як потужні інструменти для оцінки генетичної варіації серед популяцій ARO та для відрізнення цього місцевого сорту від двох інших місцевих сортів червоної цибулі Південної Італії. Крім того, ми оцінили гостроту та вміст розчинної твердої речовини, щоб оцінити смак ARO у зв’язку з ринковим попитом.
результати
Створення колекції зародкової плазми червоної цибулі Acquaviva та морфологічна характеристика
Для створення колекції зародкової плазми ARO було використано насіння 13 популяцій місцевого сорту ARO, подарованих фермерами в рамках проекту BiodiverSO Apulia Region.
Морфологічні дескриптори, пов’язані з цибулиною, шкіркою та м’якоттю, були зібрані на зародковій плазмі ARO та на трьох місцевих сортах цибулі, два належали до місцевого сорту «Червона цибуля Тропеа» (TRO), а один – до місцевого сорту «Монторо мідна цибуля» (MCO) (рис. 1). Усі цибулини ARO були плоскими і характеризувались червоною зовнішньою шкіркою та м’якоттю з різними відтінками червоного. Навпаки, м’якоть цибулин TRO була повністю червоною, тоді як м’якоть цибулин MCO була погано пігментована (таблиця S1). Біохімічний аналіз дозволив оцінити вміст твердої розчинної речовини та гостроту. Як повідомляється в табл 1, середні значення твердого розчинного вмісту цибулин у популяціях ARO становили 7.60 і коливалися від 6.00 (ARO12) до 9.50° Brix (ARO11 і ARO13). Це значення було вище, ніж оцінене для старовинних сортів TRO та MCO (4.25 та 6.00° Brix, відповідно).

Таблиця 1. Вміст твердих розчинних речовин і значення гостроти, оцінені в популяціях «Червона цибуля Acquaviva» (ARO), «Червона цибуля Тропеа» (TRO) і «Монторо Медна цибуля» (MCO) *.
| КОД | Вміст розчинних твердих речовин (Брікс) | Гострота (pmolg-1 FW) | ||
| Середня | CV y (%) | Середня | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 аб * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 XNUMX XNUMX БХД | 9.42 | 5.28 аб | 22.88 |
| ARO4 | 7.50 XNUMX XNUMX БХД | 0.00 | 6.97 | 3.74 |
| ARO 5 | 7.50 XNUMX XNUMX БХД | 0.00 | 6.80 | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 аб | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 аб | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 аб | 6.57 |
| ARO11 | 9.50 | 7.44 | 5.54 аб | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 аб | 9.70 |
| ARO13 | 9.50 | 7.44 | 6.63 | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 аб | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 аб | 4.79 |
* Значення з однаковими літерами у верхньому та нижньому регістрах статистично не відрізняються на 0.01P або 0.05P відповідно (тест SNK). y Коефіцієнт варіації.
Середнє значення гостроти ARO, оцінене за допомогою вмісту піровиноградної кислоти, становило 6.00, коливалося від 4.51 пмоль г-1 FW (ARO6) до 7.04 (ARO8). Це значення було вище, ніж оцінене для TRO та MCO старовинних сортів (3.54 pmol g-1 FW і 4.18 пмоль g-1 FW відповідно).
Поліморфізм SSR і генетичні зв'язки між зразками
У цьому дослідженні 11 із 37 протестованих комбінацій праймерів SSR забезпечили поліморфізм одного локусу, тобто давали щонайбільше два продукти ампліфікації в одній особині. Загалом у 55 осіб було виявлено 320 алелів з кількістю алелів на локус від 2 (ACM147 і ACM 504) до 11 (ACM132) і середнім значенням 5 алелів (табл. 2). В окремих популяціях число алелів (Na) коливалося від 1.94 (ACM147 і ACM504) до 5.38 (ACM132), тоді як ефективне число алелів (Ne) коливалося від 1.41 (ACM152) до 2.82 (ACM449). Розбіжності між значеннями Na і Ne були обумовлені наявністю алелів з низькою частотою в популяціях і переважанням лише кількох алелів. Найвище спостережене значення гетерозиготності (Ho) було виділено для ACM138 і ACM449 (0.62), тоді як найнижче було пов’язано з ACM152 (0.25). Очікувана гетерозиготність (He), яка відповідає теоретичному очікуванню в панміктичній популяції, коливалася від 0.37 (ACM504) до 0.61 (ACM132, ACM138 і ACM449). Індекс фіксації Райта (Fis) показав значення, близькі до нуля (в середньому 0.05) для всіх маркерів, що вказує на подібні значення між спостережуваним і очікуваним рівнями гетерозиготності, як і очікувалося для ауткросингових видів. Ефективність індивідуального SSR-маркера в генетичному фінгерпринтингу оцінювали за індексом вмісту поліморфної інформації (PIC) із середнім значенням 0.48 і варіювали від 0.33 (ACM504) до 0.67 (ACM132). Інший індекс ефективності, інформаційний індекс Шеннона (I) показав середнє значення 0.84, а припущені значення коливалися від 0.45 (ACM152) до 1.20 (ACM132).
Таблиця 2. Особливості поліморфізму 11 маркерів SSR, що використовуються для оцінки генетичного різноманіття в популяціях ARO, TRO та MCO. Загальна кількість алелів (Na), діапазон розміру смуги та індекс вмісту поліморфної інформації (PIC) Зверніться до загального набору з 320 осіб, генотипованих у цьому дослідженні. Кількість алелів (Na), кількість ефективних алелів (Ne), спостережувана гетерозиготність (Ho), очікувана гетерозиготність (He), індекс фіксації (Fis), а інформаційний індекс Шеннона (I) відноситься до середніх значень, розрахованих на основі 16 популяцій, кожна з яких складається з 20 осіб.
| Локус. | Загальний Na | Діапазон розмірів (bp) | PIC | Середня | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Середня | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Серед популяцій ARO3, ARO6, ARO8, ARO10, TRO1 і MCO продемонстрували високий рівень генетичної варіації (Ho > 0.5), тоді як найнижча різноманітність спостерігалася в популяції ARO7 (Ho = 0.27) (Додаткова таблиця S2). Загалом, усі зразки демонструють Fis значення, близькі до нуля (Fis середнє значення = 0.054), як і очікувалося за умов випадкового спаровування.
Аналіз молекулярної варіації та генетичної структури
AMOVA обчислила ієрархічний розподіл генетичної варіації між популяціями та всередині них. Результати підкреслили значну частку генетичної варіації в популяціях (87%). Різниця між популяціями, 13%, була дуже значною (P < 0.001) (табл 3). Попарні значення параметра Fpt, аналогічного індексу фіксації Райта Fst, у діапазоні від 0.002 (ARO2/ARO10) до 0.468 (ARO7/TRO2), були значущими (P < 0.05), за винятком дев'яти парних порівнянь (додаткова таблиця S3).
Таблиця 3. Аналіз молекулярної дисперсії 320 генотипів із 16 популяцій Allium cepa L.
| Source | df | Сума квадратів | Оцінка дисперсії | Дисперсія (%) | Fpt | P |
| Серед популяцій | 15 | 458.63 | 1.16 | 13% | ||
| У популяціях | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Усього: | 319 | 2731.62 | 8.66 |
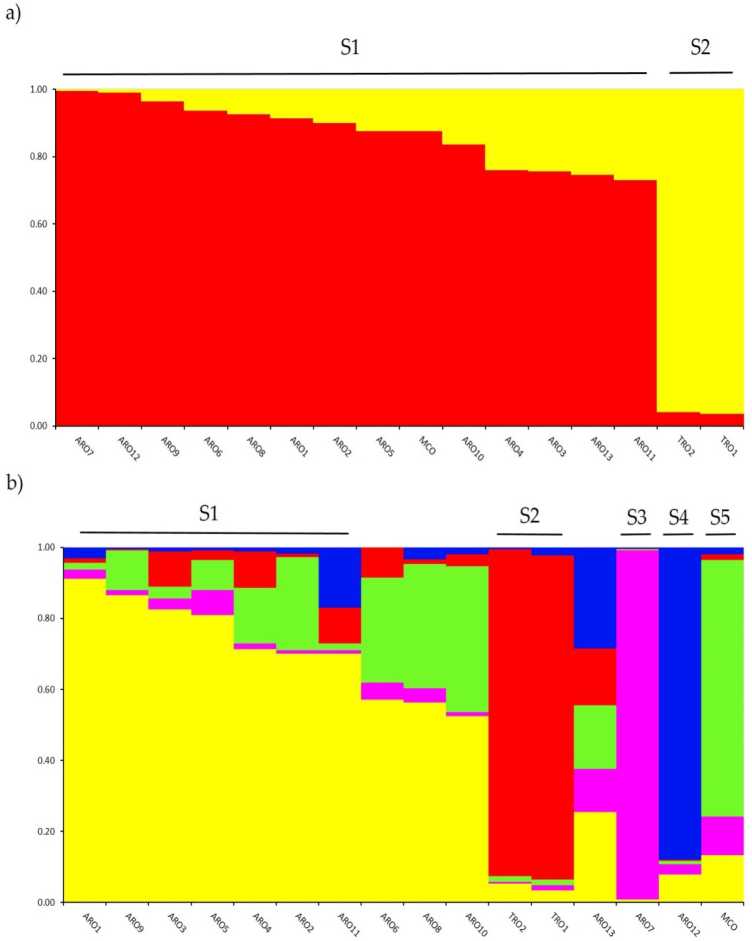
Дослідження генетичної структури в A. cepa колекцію, генотиповану в цьому дослідженні, проводили за допомогою кластеризаційного аналізу на основі моделі домішків, реалізованого в програмному забезпеченні STRUCTURE. Метод Evanno AK запропонував поділ на два кластери (K = 2) як найбільш інформативний для нашої набору даних,з юe наступний найвищий пеак у К = 5 (доповнений малюнок S1). для К = 2, aл.сopulations were assigned до оnіf два кластери з коефіцієнт rnernbertoip (q) > 0.7. Як сhown в Рисунок 2a, перший кластер (під назвою S1) включав MCO та всі популяції ARO, тоді як кластер S2 згрупував дві популяції TRO. При K = 5, що забезпечує більш глибокий опис набору даних (рис 2b), 75% зразків були віднесені до одного з п’яти кластерів. Розділення між ARO (S1) і TRO (S2) було підтверджено, хоча деякі популяції ARO були змішані (q <0.7) або згруповані окремо в двох нових кластерах S3 і S4 (ARO7 і ARO12, відповідно). Цікаво, що промисловий тип MCO утворив окремий кластер (S5), відокремлений від апулійської червоної цибулі.
Генетичні зв'язки між популяціями
Поліморфізм SSR дозволив скласти дендрограму генетичного різноманіття, а результати філогенетичного аналізу наведені на рис. 3a. Тут колекція зародкової плазми була розділена на п’ять груп, які сильно підтримуються початковими значеннями. Популяції ARO7 і ARO12 були негайно відокремлені від решти популяцій і утворили два різних кластери. Третій кластер включав дві комерційні популяції TRO, тоді як четвертий вузол розділяв MCO з одинадцяти популяцій ARO. Генетичний зв'язок між популяціями був додатково досліджений за допомогою аналізу головних координат (PCoA) (рис. 3b). Як зазначалося раніше, популяції ARO були згруповані тісно, за винятком ARO12 і ARO7, які з’являлися в ізольованих позиціях на графіку PCoA. Два TRO і популяції MCO були розкидані в нижній правій частині графіка.
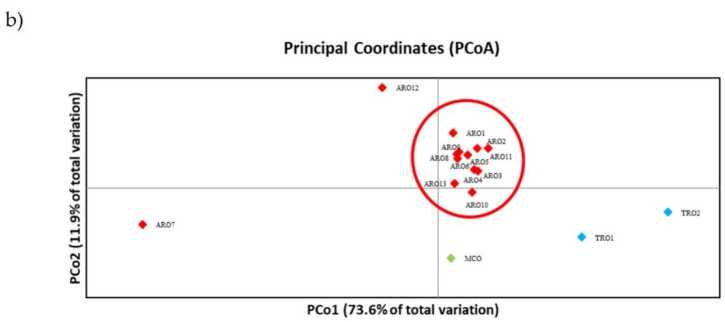
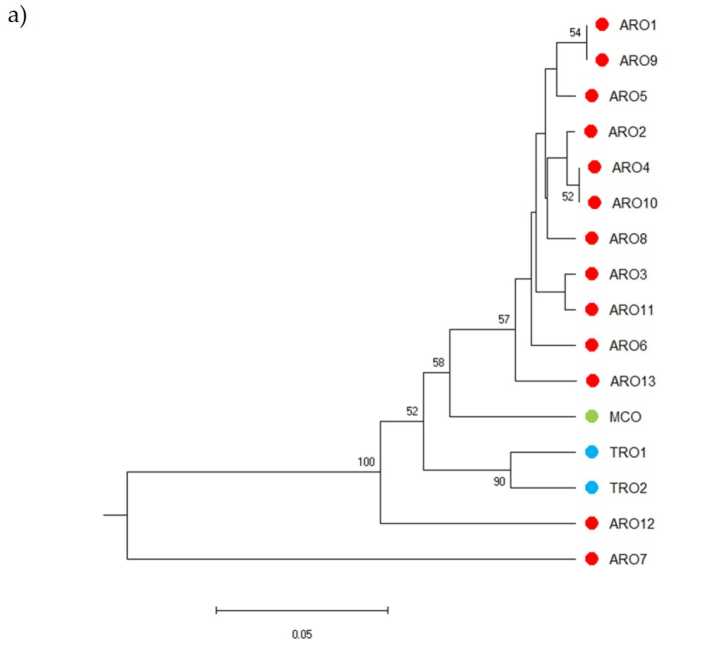
Малюнок 3. Генетична різноманітність серед 16 A. cepa популяції, охарактеризовані в цьому дослідженні, на основі їх профілю SSR. (a) UPGMA дендрограма генетичної відстані. Значення підтримки Bootstrap >50 вказуються над відповідними вузлами; (b) аналіз головних компонентів (PCoA). Кластер, обведений червоним, повністю збігався з групою, створеною за допомогою філогенетичного аналізу та складеною з 11 зразків ARO.
Обговорення
Серед великого агробіорізноманіття, яке традиційно вирощується в Південній Італії, старовинні сорти цибулі представляють нішеві продукти, які необхідно зберегти від ризику генетичної ерозії та загрози заміни сучасними сортами. У рамках регіонального проекту BiodiverSO, спрямованого на збір, характеристику, популяризацію та охорону генетичних ресурсів регіону Апулія, тісно пов’язаних із місцевою спадщиною, ми створили колекцію насіння 13 популяцій ARO landrace. Ми повідомили про першу оцінку варіації ARO з точки зору поліморфізму ДНК та двох біохімічних параметрів, вмісту розчинної твердої речовини та піровиноградної кислоти, пов’язаних зі смаковими характеристиками та важливих для прийняття свіжих сирих продуктів. Крім того, дані про старовинний сорт ARO порівнювали з даними, зібраними щодо двох інших пігментованих сортів цибулі, з якими часто помилялися.
Біохімічний аналіз підкреслив солодкість 13 популяцій ARO, пов’язану з високим вмістом розчинних твердих речовин і середньою гостротою, відповідно до рекомендацій промисловості солодкої цибулі [31]. Цибулини ARO були солодшими, ніж у старовинних сортів TRO та MCO, і демонстрували дещо вищу гостроту. Однак солодкість цибулі пояснюється балансом між вмістом цукру та гостротою, тому ця характеристика може бути корисною для підтримки відбору цінних генотипів, який зазвичай здійснюється фермерами лише на основі морфології.
Було підтверджено, що маркери SSR є корисним інструментом для розрізнення генотипів, хоча й зібрані у вузькій зоні вирощування, такій як місто Аквавіва-делле-Фонті. Вибрані маркери відображали більшу кількість алелів, ніж раніше повідомлені маркери [43] та [44], але нижче, ніж маркери, зазначені [45]. Крім того, 50% нашого набору маркерів показали значення індексу PIC більше 0.5, що виявилося придатним для розрізнення популяцій у колекції, як запропоновано [46]. Оцінка різноманітності в популяціях виявила подібні значення між Ho і He, що призвело до низького Fis значення. Це узгоджується з природою ауткросингу A. cepa, яка серйозно страждає від інбридингової депресії [47]. Загальний Fis значення, розраховане в популяціях цибулі, розглянутих у цьому дослідженні (0.054), було нижчим, ніж раніше повідомлене [45] (0.22) і майже ідентичний знайденому [31] (0.08) і [48] (0.00), які оцінювали генетичне різноманіття місцевих сортів цибулі з північного заходу Іспанії та Нігеру відповідно. Варті уваги рівні гетерозиготності в популяціях ARO підкріплюють уявлення про те, що Апулія є центром різноманітності для багатьох садових видів [32, 42, 49-51].
AMOVA підкреслила, що більшість молекулярних варіацій у колекції, генотипованій у цьому дослідженні, знаходяться в популяціях. Однак значна генетична диференціація серед популяцій (FPT цінностей) виявлено виникнення генетичної стратифікації. Насправді, хоча наші результати вказують на наявність генетичної однорідності в більшості популяцій ARO, утворюючи чітко визначений кластер, популяції ARO7 і ARO12 продемонстрували чітко виражений генетичний профіль. Цей результат міг бути пов’язаний з різним походженням насіння, використаного двома фермерами, з яких були зібрані популяції. Більше того, виходячи з отриманих результатів, місцевий сорт ARO можна вважати чітко відмінним на генетичному рівні від старовинних сортів TRO та MCO. У недавньому дослідженні [29] оцінив генетичне різноманіття кількох місцевих сортів італійської цибулі, включаючи «Аквавіва», «Тропеа» та «Монторо». Хоча автори використовували SNP-маркери для оцінки генетичного різноманіття ширшої колекції цибулі, генотипування не змогло відрізнити «Acquaviva» від цибулі «Tropea» і «Montoro». Ймовірно, ця розбіжність зумовлена низьким середнім значенням PIC (0.292), що свідчить про помірну загальну інформативність досліджуваних локусів, як стверджує [29]. Крім того, щоб дослідити наявність підструктури в їхньому італійському кластері, було б краще проаналізувати італійські генотипи окремо від решти колекції. Ймовірно, це дозволило б візуалізувати модель генетичного різноманіття, пов’язану з географічною стратифікацією або ознаками під час емпіричного відбору.
На завершення це дослідження представляє вичерпний звіт про сорт цибулі місцевої культури, пов’язаний з місцевою культурною спадщиною та має економічне значення для фермерів. Наші результати підкреслюють, що, за кількома винятками, ARO характеризується чітко визначеним генофондом, який заслуговує на збереження від ризику генетичної ерозії. Тому створення репрезентативної колекції цього цінного джерела генетичного різноманіття було надзвичайно важливим. Нарешті, генетична та фенотипова характеристика ARO може бути корисною для отримання знаків якості від Європейського Союзу.
Матеріали та методи
Збір зародкової плазми, рослинний матеріал та екстракція ДНК
Набір із 13 популяцій місцевого сорту ARO було отримано в рамках проекту регіону Апулія (BiodiverSO: https://www.biodiversitapuglia.it/), через серію місій, здійснених у «Acquaviva delle Fonti», невеликому містечку Апулії в провінції Барі, Італія. Місця збору кожного екземпляра були нанесені на карту за допомогою Географічної інформаційної системи (ГІС) і представлені в табл 4. Крім того, дві популяції з місцевої породи TRO та одна популяція з місцевої породи MCO були включені в це дослідження та використані як посилання. Весь рослинний матеріал вирощували в однакових умовах навколишнього середовища на експериментальній фермі «P Martucci» Університету Барі (41° 1'22.08″ пн.ш., 16°54'25.95″ сх.д.), у захисній клітці, щоб уникнути перехресного запилення серед популяцій і забезпечення внутріпопуляційного запилення за допомогою мух (Люцілія Цезар). 16 популяцій були охарактеризовані за ознаками, пов’язаними з розміром і формою цибулини, кольором шкірки та м’якоті (таблиця S1). Крім того, аналіз вмісту твердих розчинних речовин проводили за допомогою ручного рефрактометра, а гостроту вимірювали у зразках цибулевого соку з додаванням 2,4-динітрофенілгідразину (0.125% v/v у 2 н. HCl) і оцінюючи абсорбцію при 420 нм, як повідомляє [31]. Для визначення наявності суттєвих відмінностей було проведено багатодіапазонний тест Дункана та тест SNK.
Таблиця 4. Список популяцій, зібраних і генотипованих у цьому дослідженні. Для кожної популяції повідомляється ідентифікаційний код, місцева назва, GPS-координата та банк генів, у якому зберігаються насіння.
| код | ІМ'Я | Координати GPS | Банк генів y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54"51.372″ N 16°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52"49.8″ N 16°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Чиполла рамата ді Монторо | - | Di.SSPA |
| y Di.SSPA, Департамент ґрунтових, рослинних і харчових наук, Університет Барі. |
Листковий матеріал 20 генотипів на популяцію відбирали та зберігали при -80 °C до використання. Для видів, багатих полісахаридами, як A. cepa, перші кроки видалення полісахариду є важливими для отримання якісної ДНК, тому початкові промивки в буфері STE (0.25 М сахарози, 0.03 М Трис, 0.05 М ЕДТА) проводили, як описано в [52]. Тотальну ДНК екстрагували за методом CTAB [53] і, нарешті, було перевірено якість і концентрацію за допомогою спектрофотометра Nano Drop 2000 UV-vis (ThermoScientific, Waltham, MA, США) і електрофорезу в 0.8% агарозному гелі.
Аналіз SSR
16 комбінацій праймерів EST-SSR, розроблених [54] і раніше перевірено в дослідженнях генетичного різноманіття [43] та [44] і 21 геномний SSR [45-55] пройшли скринінг для оцінки їх придатності (додаткова таблиця S4). Генотипування проводили за допомогою економічного методу флуоресцентного мічення, за якого хвіст M13 додається до кожного прямого праймера SSR [56]. Суміші для ПЛР готували у вигляді 20 г реакційної суміші, що містила: 50 нг загальної ДНК, 0.2 мМ суміші dNTP, 1X буфера для реакції ПЛР, 0.8 ОД ДНК-полімерази DreamTaq (Thermo Scientific, Waltham, MA, США), 0.16 гМ зворотного праймера , 0.032 гМ прямого праймера, розширеного послідовністю M13 (5'-TGTAAAACGACGGCCAGT-3'), і 0.08 гМ універсального праймера M13, міченого флуоресцентними барвниками FAM або NED (Sigma-Aldrich, Сент-Луїс, Міссурі, США). Реакції ПЛР проводили в термоциклері SimpliAmp (Applied Biosystems, Каліфорнія, США) за таких умов для більшості пар праймерів: 94 °C протягом 5 хв, 40 циклів при 94 °C протягом 30 с, 58 °C. протягом 45 с і 72 °C протягом 45 с і кінцевої елонгації при 72 °C протягом 5 хв. Що стосується ACM446 і ACM449, точдаун ПЛР було застосовано з відпалом від 60 °C до 55 °C протягом 10 циклів, 30 циклів при 55 °C, з подальшим остаточним подовженням на 5 хвилин при 72 °C. Продукти ПЛР завантажували в 96-лунковий планшет і змішували з 14 г Hi-Di Formamide (Life Technologies, Карлсбад, Каліфорнія, США) і 0.5 г GeneScan 500 ROX Size Standard (Life Technologies, Карлсбад, Каліфорнія, США). Амплікони були розділені за допомогою машини для капілярного секвенування ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Карлсбад, Каліфорнія, США), де алелі оцінювали як співдомінантні та розподіляли за допомогою програмного забезпечення GeneMapper версії 3.7.
Програмне забезпечення GenAlEx 6.5 [57] і Cervus 3.0.7 [58] використовувалися для оцінки кількості алелів (Na), кількості ефективних алелів (Ne), спостережуваної гетерозиготності (Ho), очікуваної гетерозиготності (He), вмісту поліморфної інформації (PIC), інформаційного індексу Шеннона (I) та індексу фіксації (Fis ) для кожного локуса SSR.
Оцінка генетичного різноманіття
Ієрархічний розподіл генетичної мінливості між популяціями цибулі та всередині них було оцінено за допомогою GenAlEx 6.5 [57] за допомогою аналізу молекулярної дисперсії (AMOVA) із завантаженням 999 для перевірки значущості. Крім того, програмне забезпечення GenAlEx 6.5 використовувалося для оцінки різноманітності в кожній популяції шляхом обчислення середнього значення Ho, He та Fis для всіх локусів SSR.
Структуру популяції було визначено за допомогою алгоритму кластеризації на основі байєсівської моделі, реалізованого в програмному забезпеченні STRUCTURE v.2.3.4 [59]. Набір даних запускався з кількома гіпотетичними кластерами (K) у межах від 1 до 10, встановлюючи десять незалежних циклів для кожного значення K. Для кожного циклу з метою перевірки узгодженості результатів було виконано 100,000 100,000 початкових періодів вигоряння та XNUMX XNUMX ітерацій ланцюга Маркова Монте-Карло (MCMC) за моделлю домішок і незалежними частотами алелів серед популяцій. Найбільш вірогідне значення К було визначено за допомогою методу АК, описаного [60], в веб-програмі STRUCTURE HARVESTER [61]. Окрему популяцію відносили до певного кластера, якщо її коефіцієнт приналежності (q-значення) був вищим за 0.7, інакше її вважали змішаним походженням.
Аналіз головних координат був проведений для того, щоб візуалізувати закономірності генетичного зв’язку між зразками, виявлені за допомогою матриці генетичної відстані Nei (додаткова таблиця S5). На основі частот алелів була побудована дендрограма генетичної дистанції за допомогою кластерного аналізу незважених парних груп із середніми арифметичними (UPGMA) у програмному забезпеченні POPTREEW [62]. Для оцінки впевненості в ієрархічній кластеризації було застосовано початкове завантаження, встановивши 100 повторних вибірок набору даних. Нарешті, програмне забезпечення MEGA X [63] використовувався як програмне забезпечення для малювання дерев.
Додаткові матеріали: Наступні дані доступні в мережі Інтернет за адресою http://www.mdpi.com/2223-7747/9/2/260/s1. Таблиця S1: Морфологічна характеристика цибулин ARO, MCO та TRO. Таблиця S2: Індекси гетерозиготності та фіксації, розраховані для місцевих сортів ARO та старовинних сортів TRO та MCO. Таблиця S3: Попарні значення параметра Fpt. Таблиця S4: Список SSR, використаних у дослідженні. Таблиця S5. Попарна популяційна матриця генетичної відстані Nei. Рисунок S1: Лінійна діаграма значень K, що змінюються з дельта K Еванно.
Внески автора: CL і LR задумали дослідження та розробили експеримент; CL та PI провели аналіз молекулярних маркерів; АРМ та ВЗ провели польові випробування; RM, SP, GR та CL були залучені до аналізу даних; RM і CL написали рукопис. Усі автори прочитали та погодилися з опублікованою версією рукопису.
Фінансування: Ця робота була профінансована Регіональним проектом Апулії «Біорізноманіття видів овочів Апулії»—Programma di Sviluppo Rurale per la Puglia 2014-2020. Місура 10—Соттомісура 10.2; грант CUP H92C15000270002, Італія.
підтвердження: Висловлюємо подяку «Azienda Agricola Iannone Anna» та «Associazione produttori della vera cipolla rossa di Acquaviva» за надання рослинних матеріалів, які використовуються в експерименті.
Конфлікт інтересів: Автори не оголошують конфлікту інтересів.
посилання
- 1. Стерн, В.Т. Скільки видів луку відомо? Kew Mag. 1992, 9, 180–182. [CrossRef]
- 2. ФАОСТАТ. Статистична база даних ФАО. Доступно онлайн: http://www.fao.org/2017 (переглянуто 8 січня 2019 р.).
- 3. Блок Е. Хімія часнику і цибулі. Sci. Am. 1985, 252, 114–119. [CrossRef]
- 4. Лі, Б.; Юнг, Дж.Х.; Кім, Г. С. Оцінка антиоксидантної активності червоної цибулі у щурів. Харчова хім. Токсикол. 2012, 50, 3912-3919. [CrossRef]
- 5. Лі С.М.; Місяць, Дж.; Chung, JH; Cha, YJ; Шин, М. Дж. Вплив багатих на кверцетин екстрактів шкірки цибулі на артеріальний тромбоз у щурів. Харчова хім. Токсикол. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Йосінарі, О.; Сіодзіма, Ю.; Ігараші, К. Ефекти екстракту цибулі проти ожиріння у цукрових діабетичних жирних щурів. Живильні речовини 2012, 4,1518-1526. [CrossRef]
- 7. Акаша, МШ; Реман, К.; Chen, S. Пряна рослина Allium cepa: Дієтична добавка для лікування цукрового діабету 2 типу. харчування 2014, 30, 1128–1137. [CrossRef] [PubMed]
- 8. Ван Ю.; Тянь, WX; Ma, XF Інгібуючі ефекти цибулі (Allium cepa L.) екстракт проліферації ракових клітин і адипоцитів шляхом інгібування синтази жирних кислот. Азіатський Pac. J. Рак Поперед. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Лай, WW; Хсу, SC; Чуе, Ф.С.; Chen, YY; Ян, JS; Лін, Дж. П.; Лієн, Дж. К.; Цай, CH; Чунг, Дж. Г. Кверцетин пригнічує міграцію та інвазію ракових клітин порожнини рота людини SAS через інгібування сигнальних шляхів NF-kappaB і матриксної металопротеїнази-2/-9. Протипухлинний Рез. 2013, 33, 1941–1950. [PubMed]
- 10. Нікастро, HL; Росс, SA; Мілнер, Дж. А. Часник і цибуля: їх властивості профілактики раку. Рак Поперед. рез. 2015, 8,181-189. [CrossRef]
- 11. Форте, Л.; Торрічеллі, П.; Боаніні, Е.; Гаццано, М.; Рубіні, К.; Фіні, М.; Bigi, A. Антиоксидантні та кісткові властивості відновлення гідроксиапатиту, функціоналізованого кверцетином: дослідження спільного культивування остеобластів-остеокластів-ендотеліальних клітин in vitro. Акта Біоматер. 2016, 32, 298-308. [CrossRef]
- 12. Ямазакі, Ю.; Івасакі, К.; Мікамі, М.; Yagihashi, A. Розподіл одинадцяти попередників смаку, похідних S-Alk(en)yl-L-цистеїну, у семи овочах Allium. Харчова наука. технол. рез. 2011, 17, 55-62. [CrossRef]
- 13. Блок, Е. Сіркоорганічна хімія роду Allium — наслідки для органічної хімії сірки. Angew. хім. Int. ред. англ. 1992, 31, 1135–1178. [CrossRef]
- 14. Гріффітс, Г.; Труман, Л.; Кроутер, Т.; Томас, Б.; Сміт, Б. Цибуля - глобальна користь для здоров'я. Фітотер. рез. 2002,16, 603-615. [CrossRef]
- 15. Швіммер, С.; Weston, WJ Ферментативний розвиток піровиноградної кислоти в цибулі як міра гостроти. Дж. Агрік. Food Chem. 1961, 9, 301-304. [CrossRef]
- 16. Кеттер, КЕТ; Randle, WM Оцінка гостроти цибулі. в Перевірені дослідження для лабораторного навчання; Karcher, SJ, Ed.; Асоціація біологічної лабораторної освіти (ABLE): Нью-Йорк, Нью-Йорк, США, 1998; Том 19, С. 177-196.
- 17. Ганелт, П. Таксономія, еволюція та історія. в Цибуля та споріднені культури, том. I. Ботаніка, фізіологія і генетика; Рабінович, HD, Брюстер, JL, Ред.; CRC Press: Бока Ратон, Флорида, США, 1990; С. 1-26.
- 18. Рабінович, HD; Курра, Л. Наука про рослинництво луку: останні досягнення; Видавництво CABI: Воллінгфорд, Великобританія, 2002.
- 19. Маллор, К.; Карраведо, М.; Естопанан, Г.; Маллор, Ф. Характеристика генетичних ресурсів цибулі (Allium cepa L.) від іспанського secondary center of diversity. Проліт. Дж. Агрік. рез. 2011, 9, 144–155. [CrossRef]
- 20. Феріолі, Ф.; D'Antuono, LF Оцінка фенольних сполук і сульфоксидів цистеїну в місцевій зародковій плазмі цибулі та шалоту з Італії та України. Жене. ресурс. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Петропулос, SA; Фернандес, А.; Баррос, Л.; Феррейра, ICFR; Ntatsi, G. Морфологічний, поживний та хімічний опис 'vatikiotiko', місцевого сорту цибулі з Греції. Харчова хім. 2015,182, 156–163. [CrossRef]
- 22. Лігуорі, Л.; Аділетта, Г.; Наццаро, Ф.; Фратіанні, Ф.; Ді Маттео, М.; Альбанезе, Д. Біохімічні, антиоксидантні властивості та антимікробна активність різних сортів цибулі в середземноморській зоні. J. Food Meas. Характер. 2019,13, 1232–1241. [CrossRef]
- 23. Ю, К.С.; Щука, Л.; Кросбі, К.; Джонс, Р.; Лесковар, Д. Відмінності гостроти цибулі залежно від сортів, середовища зростання та розміру цибулини. наук. Hortic. 2006,110, 144–149. [CrossRef]
- 24. Біск, Н.; Пернер, Х.; Шварц, Д.; Джордж, Е.; Кро, Л. В.; Rohn, S. Розподіл кверцетин-3, 4'-O-диглюкозиду, кверцетин-4'-O-моноглюкозиду та кверцетину в різних частинах цибулини (Allium cepa L.) під впливом генотипу. Харчова хім. 2010,122, 566-571. [CrossRef]
- 25. Карузо, Г.; Конті, С.; Вілларі, Г.; Борреллі, К.; Melchionna, G.; Мінутоло, М.; Руссо, Г.; Amalfitano, C. Вплив часу пересадки та густоти рослин на врожайність, якість та вміст антиоксидантів у цибулі (Allium cepa L.) на півдні Італії. наук. Hortic. 2014,166, 111–120. [CrossRef]
- 26. Перес-Грегоріо, MR; Регейро, Ж.; Сімал-Гандара, Дж.; Родрігес, А.С.; Алмейда, DPF Збільшення доданої вартості цибулі як джерела антиоксидантних флавоноїдів: критичний огляд. Критикувати Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Понл, Т.; Швайггерт, Р.М.; Карл, Р. Вплив методу культивування та вибору сорту на розчинні вуглеводи та гострі принципи в цибулі (Allium cepa Л.). Дж. Агрік. Food Chem. 2018, 66, 12827–12835. [CrossRef] [PubMed]
- 28. Тедеско, І.; Карбоне, В.; Spagnuolo, C.; Мінасі, П.; Russo, GL Ідентифікація та кількісне визначення флавоноїдів з двох південноіталійських сортів Allium cepa L., Tropea (червона цибуля) і Montoro (мідна цибуля), а також їх здатність захищати еритроцити людини від окисного стресу. Дж. Агрік. Food Chem. 2015, 63, 5229-5238. [CrossRef]
- 29. Віллано К.; Еспозіто, С.; Каруччі, Ф.; Фрусчанте, Л.; Карпуто, Д.; Аверсано, Р. Високопродуктивне генотипування цибулі розкриває структуру генетичного різноманіття та інформативні SNP, корисні для молекулярної селекції. мол. Порода. 2019, 39, 5. [CrossRef]
- 30. Меркаті, Ф.; Лонго, С.; Пома, Д.; Араніті, Ф.; Лупіні, А.; Маммано, М.М.; Фіоре, MC; Абенаволі, MR; Sunseri, F. Генетична варіація італійських томатів тривалого зберігання (Паслін lycopersicum L.) збір за допомогою SSR і морфологічних ознак плодів. Жене. ресурс. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Гонсалес-Перес, С.; Маллор, К.; Гарсес-Клавер, А.; Меріно, Ф.; Табоада, А.; Рівера, А.; Помар, Ф.; Перович, Д.; Silvar, C. Вивчення генетичного різноманіття та якісних ознак у колекції цибулі (Allium cepa L.) старовинні сорти з північно-західної Іспанії. Генетика 2015, 47, 885-900. [CrossRef]
- 32. Лотті К.; Iovieno, P.; Чентомані, І.; Маркотріджано, AR; Фанеллі, В.; Міміола, Г.; Суммо, К.; Паван, С.; Ricciardi, L. Генетична, біоагрономічна та харчова характеристика листової капусти (Brassica oleracea L. вар. ацефала) різноманітність в Апулії, Південна Італія. різноманітність 2018,10, 25. [CrossRef]
- 33. Бардаро, Н.; Маркотріджано, AR; Бракуто, В.; Маццео, Р.; Ріккарді, Ф.; Лотті, С.; Паван, С.; Ricciardi, L. Генетичний аналіз стійкості до Orobanche crenata (Форск.) в горошині (Pisum sativum L.) низькостриголактонова лінія. J. Plant Pathol. 2016, 98, 671-675.
- 34. Вако, Т.; Цуказакі, Х.; Ягучі, С.; Ямашіта, К.; Іто, С.; Шигьо, М. Картування локусів кількісних ознак для часу висадки цибулі в пучки (Allium fistulosum Л.). Euphytica 2016, 209, 537-546. [CrossRef]
- 35. Дака, Н.; Мухопадхяй, А.; Парітош, К.; Гупта, В.; Пентал, Д.; Прадхан, А. К. Ідентифікація генних SSR та побудова карти зв’язків на основі SSR у Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Анандхан, С.; Моте, С.Р.; Гопал, Дж. Оцінка ідентичності сорту цибулі за допомогою маркерів SSR. Seed Sci. технол. 2014, 42, 279-285. [CrossRef]
- 37. Мітрова, К.; Свобода, П.; Ovesna, J. Вибір і перевірка набору маркерів для диференціації сортів цибулі з Чеської Республіки. Чех Ж. Жене. Порода рослин. 2015, 51, 62-67. [CrossRef]
- 38. Ді Рієнцо, В.; Міацці, М.М.; Фанеллі, В.; Сабетта, В.; Montemurro, C. Збереження та характеристика біорізноманіття зародкової плазми оливи Апулії. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Маллор, С.; Арнедо-Андрес, А.; Гарсес-Клавер, А. Оцінка генетичного різноманіття іспанської мови Allium cepa старовинні сорти для розведення цибулі ріпчастої за мікросателітними маркерами. наук. Hortic. 2014,170, 24–31. [CrossRef]
- 40. Рівера, А.; Маллор, К.; Гарсес-Клавер, А.; Гарсіа-Уллоа, А.; Помар, Ф.; Silvar, C. Оцінка генетичного різноманіття цибулі (Allium cepa L.) місцеві сорти з північно-західної Іспанії та порівняння з європейською мінливістю. NZJ Crop Hortic. 2016, 44, 103–120. [CrossRef]
- 41. Де Джованні К.; Паван, С.; Таранто, Ф.; Ді Рієнцо, В.; Міацці, М.М.; Маркотріджано, AR; Мангіні, Г.; Монтемурро, К.; Ріккарді, Л.; Lotti, C. Генетична варіація глобальної колекції зародкової плазми нуту (Cicer arietinum L.), включаючи італійські зразки, яким загрожує генетична ерозія. фізіол. мол. Biol. Рослини 2017, 23, 197–205. [CrossRef]
- 42. Маццео, Р.; Моргезе, А.; Соннанте, Г.; Зулуага, DL; Паван, С.; Ріккарді, Л.; Lotti, C. Генетичне різноманіття брокколі рабе (Brassica rapa L. subsp. сильвестріс (L.) Janch.) з Південної Італії. наук. Hortic. 2019, 253, 140–146. [CrossRef]
- 43. Якше, М.; Мартін, В.; Маккаллум, Дж.; Havey, M. Однонуклеотидні поліморфізми, інделі та прості повтори послідовності для ідентифікації сорту цибулі. J. Am. Соц. Hortic. Sci. 2005,130, 912-917. [CrossRef]
- 44. Маккаллум Дж.; Томсон, С.; Пітер-Джойс, М.; Кенел, Ф. Аналіз генетичного різноманіття та розвиток маркера однонуклеотидного поліморфізму в культивованій цибулі ріпчастої на основі маркерів експресованої послідовності та простих маркерів повторення послідовності. J. Am. Соц. Hortic. Sci. 2008,133, 810-818. [CrossRef]
- 45. Болдуін, С.; Пітер-Джойс, М.; Райт, К.; Чен, Л.; Маккаллум, Дж. Розробка надійних геномних простих маркерів повторення послідовності для оцінки генетичного різноманіття всередині та серед цибулі ріпчастої (Allium cepa L.) населення. мол. Порода. 2012, 30, 1401–1411. [CrossRef]
- 46. Де Вуді, Дж.А.; Ханікатт, Р.Л.; Skow, LC Мікросупутникові маркери білохвостих оленів. Дж. Херед. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Ходададі, М.; Хасанпанах, Д. Іранська цибуля (Allium cepa L.) реакція сортів на інбридингову депресію. Всесвітня апл. наук. Дж. 2010,11, 426-428.
- 48. Абду, Р.; Бакассо, Ю.; Сааду, М.; Baudoin, JP; Харді, О.Я. Генетичне різноманіття цибулі Нігер (Allium cepa L.) оцінюють за допомогою простих маркерів повторення послідовності (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Паван, С.; Лотті, С.; Маркотріджано, AR; Маццео, Р.; Бардаро, Н.; Бракуто, В.; Ріккарді, Ф.; Таранто, Ф.; Д'Агостіно, Н.; Скіавуллі, А.; та ін. Окремий генетичний кластер у культивованому нуті, як виявлено за допомогою виявлення загальногеномних маркерів і генотипування. Геном рослин 2017, 2017,10. [CrossRef]
- 50. Паван, С.; Маркотріджано, AR; Сіані, Е.; Маццео, Р.; Зонно, В.; Руджері, В.; Лотті, С.; Ricciardi, L. Генотипування шляхом секвенування дині (Cucumis melo L.) колекція зародкової плазми з вторинного центру різноманітності висвітлює моделі генетичної варіації та геномні особливості різних генофондів. BMC Genom. 2017, 18, 59. [CrossRef]
- 51. Ді Рієнцо, В.; Сіон, С.; Таранто, Ф.; Д'Агостіно, Н.; Монтемурро, К.; Фанеллі, В.; Сабетта, В.; Boucheffa, S.; Таменджарі, А.; Паскуалоне, А.; та ін. Генетичний потік серед популяції маслин в Середземноморському басейні. Пер Дж. 2018, 6. [CrossRef]
- 52. Пастух Л.Д.; McLay, TG Два протоколи мікромасштабу для ізоляції ДНК із багатої полісахаридами рослинної тканини. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Дойл, Дж. Дж.; Дойл, Дж. Л. Виділення ДНК рослин зі свіжої тканини. Сфокусувати 1990,12, 13–14.
- 54. Кул, Дж. К.; Чунг, Ф.; Цяопін, Ю.; Мартін, В.; Зевді, Ю.; Маккаллум, Дж.; Катанах, А.; Резерфорд, П.; Мийка, КЦ; Єндерек, М.; та ін. Унікальний набір із 11,008 XNUMX міток експресованої послідовності цибулі показує експресовану послідовність і геномні відмінності між однодольними рядами asparagales і poales. Рослинна клітина 2004,16, 114-125. [CrossRef]
- 55. Кім, Х.Дж.; Лі, HR; Хюн, JY; Пісня, KH; Кім, KH; Кім, JE; Гур, CG; Harn, CH Розробка маркерів для тестування генетичної чистоти цибулі за допомогою SSR Finder. Корейська Ж. Порода. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Шульке, М. Економічний метод флуоресцентного мічення фрагментів ПЛР. Нац. Біотехнол. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Піколл, Р.; Smouse, PE GenAlEx 6.5: Генетичний аналіз у Excel. Популяційно-генетичне програмне забезпечення для навчання та досліджень: оновлення. біоінформатика 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Калиновський С.Т.; Конусність, ML; Маршалл, TC Перегляд того, як комп’ютерна програма CERVUS враховує помилки генотипування, підвищує успіх у встановленні батьківства. мол. Ecol. 2007,16, 1099–1106. [CrossRef]
- 59. Прітчард, Дж. К.; Стівенс, М.; Розенберг Н.А.; Доннеллі, П. Картування асоціацій у структурованих сукупностях. Am. Дж. Хум. Жене. 2000, 67, 170-181. [CrossRef]
- 60. Еванно, Г.; Regnaut, S.; Goudet, J. Виявлення кількості кластерів індивідуумів за допомогою програмного забезпечення STRUCTURE: A simulation study. мол. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61 Ерл Д.; VonHoldt, B. STRUCTURE HARVESTER: Веб-сайт і програма для візуалізації результатів STRUCTURE і впровадження методу Еванно. Консерв. Жене. ресурс. 2011, 4. [CrossRef]
- 62. Такезакі, Н.; Ней, М.; Тамура, К. POPTREEW: Веб-версія POPTREE для побудови популяційних дерев із даних частоти алелів і обчислення деяких інших величин. Мол. Біол. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Кумар, С.; Стечер, Г.; Лі, М.; Князь, C.; Тамура, К. MEGA X. Молекулярний еволюційно-генетичний аналіз на різних обчислювальних платформах. Мол. Біол. Evol. 2018, 35, 1547–1549. [CrossRef]